3 méthodes passionnantes utilisées par les chimistes pour synthétiser des composés cette année
par Bethany Halford
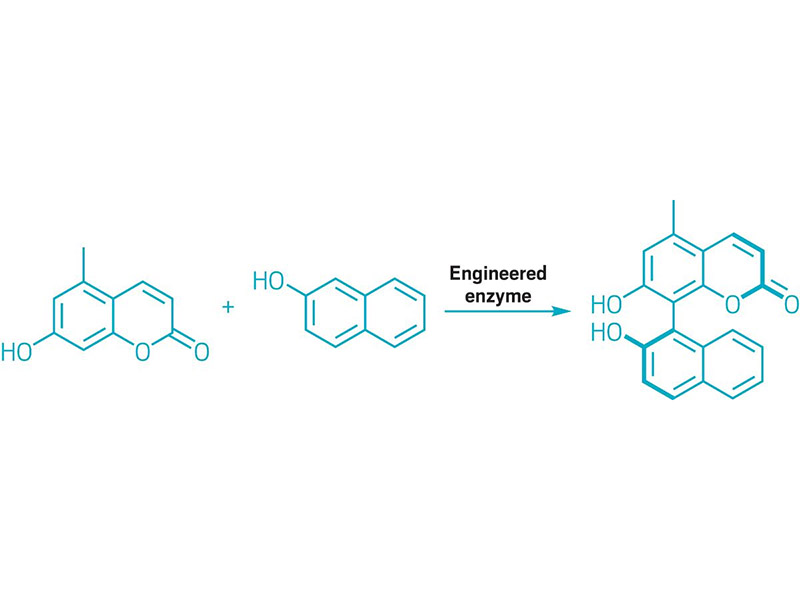
DES ENZYMES ÉVOLUÉES ONT CONSTRUIT DES LIAISONS BIARYLIQUES
Schéma illustrant un couplage biaryle catalysé par une enzyme.
Les chimistes utilisent les molécules biaryles, composées de groupes aryle liés par une simple liaison, comme ligands chiraux, éléments de base pour la construction de matériaux et produits pharmaceutiques. Cependant, la synthèse du motif biaryle par des réactions catalysées par des métaux, telles que les couplages croisés de Suzuki et de Negishi, nécessite généralement plusieurs étapes pour obtenir les partenaires de couplage. De plus, ces réactions catalysées par des métaux sont moins efficaces pour la synthèse de biaryles encombrants. S'inspirant de la capacité des enzymes à catalyser des réactions, une équipe dirigée par Alison RH Narayan de l'Université du Michigan a utilisé l'évolution dirigée pour créer une enzyme cytochrome P450 capable de construire une molécule biaryle par couplage oxydatif de liaisons carbone-hydrogène aromatiques. L'enzyme lie des molécules aromatiques pour former un stéréoisomère autour d'une liaison à rotation entravée (représentée). Les chercheurs pensent que cette approche biocatalytique pourrait devenir une transformation courante pour la fabrication de liaisons biaryles (Nature 2022, DOI : 10.1038/s41586-021-04365-7).

RECETTE DES AMINES TERTIAIRES UTILISANT UN PEU DE SEL
Le schéma illustre une réaction permettant de transformer des amines secondaires en amines tertiaires.
Le mélange de catalyseurs métalliques avides d'électrons avec des amines riches en électrons détruit généralement les catalyseurs ; par conséquent, les réactifs métalliques ne peuvent être utilisés pour synthétiser des amines tertiaires à partir d'amines secondaires. M. Christina White et ses collègues de l'Université de l'Illinois à Urbana-Champaign ont découvert qu'ils pouvaient contourner ce problème en ajoutant un agent oxydant à leur réaction. En transformant les amines secondaires en sels d'ammonium, les chimistes ont constaté qu'ils pouvaient faire réagir ces composés avec des oléfines terminales, un oxydant et un catalyseur de sulfoxyde de palladium pour créer une multitude d'amines tertiaires présentant divers groupes fonctionnels (exemple illustré). Les chimistes ont utilisé cette réaction pour fabriquer les médicaments antipsychotiques Abilify et Semap et pour transformer des médicaments existants qui sont des amines secondaires, comme l'antidépresseur Prozac, en amines tertiaires, démontrant ainsi comment les chimistes pourraient fabriquer de nouveaux médicaments à partir de médicaments existants (Science 2022, DOI : 10.1126/science.abn8382).
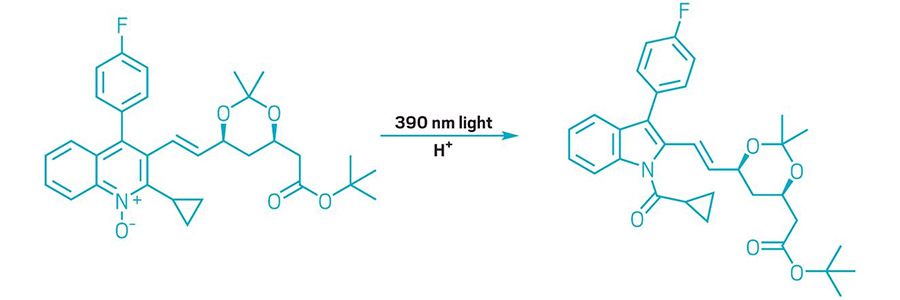
AZAARENES A SUBI UNE CONTRAINTE DE CARBONE
Le schéma montre un N-oxyde de quinoléine transformé en N-acylindole.
Cette année, les chimistes ont enrichi le répertoire de l'édition moléculaire, un ensemble de réactions permettant de modifier la structure centrale de molécules complexes. À titre d'exemple, des chercheurs ont mis au point une transformation utilisant la lumière et un acide pour cliver un atome de carbone d'azaarènes à six chaînons présents dans les N-oxydes de quinoléine, formant ainsi des N-acylindoles à cinq chaînons (exemple illustré). Cette réaction, développée par l'équipe de Mark D. Levin à l'Université de Chicago, s'inspire d'une réaction utilisant une lampe à mercure, qui émettait de la lumière à plusieurs longueurs d'onde. Levin et ses collègues ont constaté qu'une diode électroluminescente émettant à 390 nm offrait un meilleur contrôle et leur permettait de généraliser la réaction aux N-oxydes de quinoléine. Cette nouvelle réaction offre aux chimistes un moyen de remodeler la structure centrale de composés complexes et pourrait aider les chimistes médicinaux à développer leurs chimiothèques de candidats médicaments (Science 2022, DOI : 10.1126/science.abo4282).
Date de publication : 19 décembre 2022

